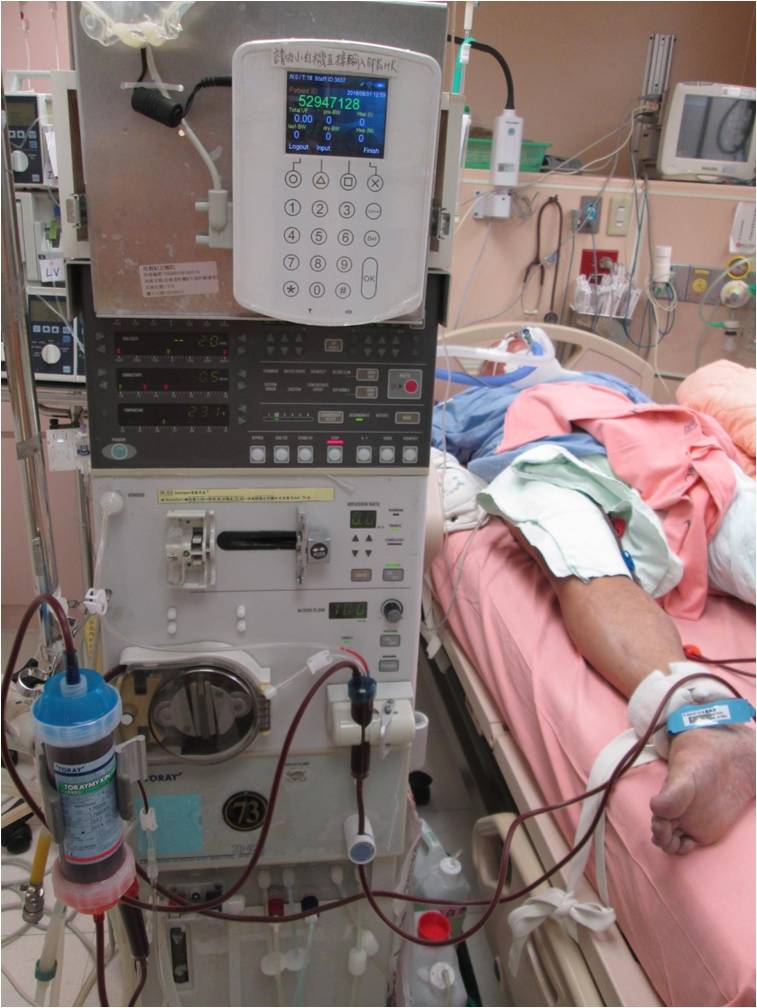
文/馬偕紀念醫院重症醫學科資深主治醫師李昭賢
重症加護單位所收治病人的病況都相當嚴峻,隨時要有醫護人員適切處理,需要更高的醫護與患者比例,提供重症的專業照護,甚至因疾病特殊需求,將重症加護單位分為不同單位,以對患有嚴重疾病或危及生命的患者,提供更專業的及時照顧。
加護單位內因此配有許多先進的治療及監測設備,以面臨瞬息萬變之病況。如心律不整,可用心律調節器或去顫器;心跳停止經急救復甦後的低溫治療,心臟衰竭可用主動脈內氣球幫浦;呼吸衰竭可用先進型呼吸器,心肺極度衰竭者可用體外循環機(葉克膜);腎臟衰竭者可用一般透析在2-4小時內完成血液透析;連續血液透析機則以24小時連續方式、低血液流速(約150-200毫升/分鐘),因其長時間連續特性,不易引起病患體內滲透壓和電解質的大幅變動,可緩慢以擴散、對流方式幫助病患排除體內多餘的水份、代謝廢物毒素,以及矯正酸鹼不平衡,適用於加護病房內血壓不穩定之重症患者;又因其長時間連續特性,不易引起病患體內滲透壓和電解質的大幅變動,常使用在急性腎衰竭合併多重器官衰竭、嚴重酸中毒、敗血性休克及嚴重水腫之病人,由於患者必須接受雙腔導管置入至大靜脈,並且他們都臥床,操作複雜需嚴密監測,較適合在加護病房內處理。
至於監測系統包括連續監測心臟的心臟監護儀,連續血氣濃度監測,巨循環及微循環血液動力學監測等。而病人則可能須通過氣管插管或氣管造口管輔助呼吸,透過鼻胃管及導尿管精確計算攝入及排出量,週邊及中心靜脈管路藉由智慧型注射泵來協助抗生素、鎮痛藥、鎮靜劑等各種藥物。
在重症加護單位治療的常見疾病,包括敗血性休克、急性呼吸窘迫症候群和其他危及生命的疾病,同時也要特別注意各類感控措施,以防繼續感染。
複雜且高死亡率高的敗血症是最常見的重症
敗血症是微生物(細菌、黴菌、病毒)侵入人體,在血液內繁殖並產生毒素引起全身性的發炎反應,較常發生於抵抗力不足的病人身上,會有發燒、心跳加速、呼吸急促、白血球上升、尿少、發紺、斑駁樣皮膚、意識變化等生命不穩定徵象,病情可能在數小時至數日內快速惡化,嚴重時會引起血壓下降、組織灌流不足,凝血功能的異常,甚至全身器官衰竭,死亡率約30-50%。
敗血症的治療包括微生物培養,使用抗微生物藥物治療以控制感染、細菌毒素消除術,血壓降低給予點滴輸液及升壓劑,置入中央靜脈導管及動脈導管以連續監測血行動力學,並施行巨循環甚至微循環監測,提供治療即時處置。
而內毒素清除療法(內毒素吸附)之適時介入或可增加病人生存之機會,利用對於細菌內毒素具有很高的親和力的特殊材質,藉由血液透析方式來吸附內毒素,將血液中內毒素的濃度降低甚至清除,改善病人的敗血症情況。因此嚴重敗血症病人,在條件允許下,可考慮使用此療法。
63歲的王先生只因左腳小傷口,發燒呼吸急促,送醫診斷為壞死性筋膜炎合併「敗血性休克」,於是施行細菌培養並使用多重抗生素治療。經大量點滴後血壓仍偏低,於是使用升壓劑來提高血壓,並急送開刀房進行筋膜切開術及清創,術後再轉至加護病房實行血液動力監測。由於持續休克併發心、肺、腎等多重器宮衰竭,遂實行細菌毒素消除術、內毒素清除療法、連續性血液淨化及4次清創,最終安全回到家庭並回歸工作崗位。藉由各種療法的及早積極介入,讓病人回歸到原本生活,這也是加護單位持續努力的目標。
急性呼吸窘迫症候群在重症醫學界極具挑戰
急性呼吸窘迫症候群是一種急性、瀰漫性肺部炎症反應,伴隨肺泡毛細血管膜通透性增加所造成的水腫、出血、肺高壓及氧合異常,可能會導致急性呼吸衰竭,嚴重者會併發敗血症或多重器官衰竭。急性呼吸窘迫症候群之預後差,在沒有人工呼吸器的年代是必然致命的疾病;而在呼吸治療及呼吸器功能逐漸發達後,病人雖不至於短期死亡,然其死亡率仍一直居高不下,約為40-70%。
患者易引發肺損傷,一般分為直接肺損傷或間接肺損傷。前者包括肺炎、大量胃酸或異物吸入、肺部創傷、肺血管炎及溺水等;肺損傷之發生應始於肺泡;後者包括敗血症、嚴重創傷、大量輸血、急性胰臟炎、嚴重燒傷等、休克,在這些情形肺部的血管內皮細胞扮演重要的角色,由感染症所造成的肺炎及敗血症為急性呼吸窘迫症候群最常見的原因,病人的預後也最差,常出現多重器官衰竭之併發症。
良好的呼吸器設定及呼吸生理的密切監控,可免於在急性發炎中因壓力性損傷進一步擴大損害,改善通氣血流灌注比例,維持其氧合作用,使呼吸肌充分休息,讓呼吸道通暢。施行俯臥治療,運用重力的影響,讓前胸通氣較佳的肺葉朝下,減少心臟對肺部的壓迫,以增加血流灌注及增加氧合作用進而改善低血氧。保守性的輸液治療可維持體液平衡及心血管系統穩定並避免肺水腫之惡化。先進的智慧型呼吸器、藥物治療及葉克膜的適時介入亦可以度過肺部急性發炎的危機。

▲智慧型呼吸器、藥物治療及葉克膜的適時介入,可提供急性呼吸窘迫症候群患者多方面的支持。
葉克膜是由「血液幫浦」(人工心臟)及「體外氧合器」(人工肺臟)之組合,血液幫浦經一導管將大靜脈內含氧量低的血液引至體外,在人工肺臟充滿氧氣後,再把高含氧量的血液經另一導管送回體內。機器可取代部分心肺功能,使受損的心肺系統獲得喘息,但無法治療導致心肺衰竭的病因。葉克膜常見的併發症包括血液快速流經管路導致的血球溶血破壞,引起肝腎衰竭。血小板耗損及大量使用抗凝血劑所造成的出血及導管感染引發的敗血症,亦可導致病人無法存活到出院。超過七天無法脫離葉克膜的病患,能存活至出院的明顯降低。
低溫治療法透過體溫控制保護腦部不受損害
一名55歲的李姓婦女在捷運站突然失去知覺,因為無心跳呼吸,路人立即心肺復甦,送至急診經電擊及高級心肺復甦後仍呈現昏迷狀態,之後接受冠狀動脈介入治療心肌梗塞,並入住重症加護單位,重症醫師評估低溫治療,將病人體溫降低到33度,幾天後李姓婦女逐漸甦醒並康復出院。
缺氧狀況下,腦內的神經元會釋放大量的穀氨酸,它是大腦最多的神經傳導物,當穀氨酸和N-甲基-D-天門冬胺酸受體接觸後會讓鈣離子進入細胞內,鈣離子啟動不同的訊息傳遞,造成細胞死亡。低溫具有神經保護作用能改善腦缺氧病人的預後。腦溫每降1度則腦代謝率約降低百分之6,並減少心臟停止後所自由基增加造成的發炎反應。
低體溫療(目標溫控治療)應在4至6小時內啟動且不宜在心肺復甦12小時後方才施行,此療法乃是藉由儀器控制在維持至少24小時的中心低溫(32°C~34°C)後,以每小時上升0.25℃的速度緩慢回溫,精密的中心體溫控制,才足以保護腦,直到體溫上升至36℃為止。但副作用也有顫抖、心律不整(常為心跳過慢)、利尿引致之電解質不平衡(低鉀血症、低磷血症、低鎂血症和低鈣血症)、高血糖、出血和免疫抑制導致肺炎風險增加。

▲低溫療法之療程,醫護人員會透過腦波、心電圖、抽血等檢查及神經學評估嚴密監控。
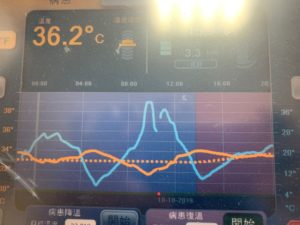
▲低溫療法的溫度顯示。
目前有三種技術可用於低體溫療法:常規冷卻法、智慧型自動體表冷卻法和智慧型自動血管內冷卻法。使用碎冰、冰袋和低溫液體灌注之常規冷卻法,具有便宜、容易取得優點;智慧型自動體表冷卻法,通過使低溫液體或空氣循環通過包覆患者的毯子或墊片來達到由體表快速降溫之裝置,優點在於容易使用且可快速啟動,同時還可提供自動反饋機制以快速精確調節控制體溫。血管內冷卻法則是使用中心靜脈降溫導管中之4℃生理食鹽水,經由熱交換方式來達到快速降溫緩慢升溫,但具有侵入性及感染、出血和血栓形成的併發症。◎